


一、联盟概况
药用辅料质量研究共享联盟是由在中华人民共和国境内注册、从事药用辅料生产,加工,销售,使用的企业和个人自愿组成的全国性、行业性、非营利性社会组织;其全称为“药用辅料质量研究共享联盟”,英文全称为“Sharing Alliance for Research and Quality of Medical Accessories”。于2018年2月10日成立,其总部位于石家庄。本联盟的发起者为石家庄凯瑞德医药科技发展有限公司。
药用辅料质量研究共享联盟为技术联盟,自愿接受药监机构领导和指导;药用辅料联盟定期发布信息,组织专题培训;联盟设置联络专员,不设常设机构。
二、联盟宗旨
以习近平同志领导的党中央为核心,遵守法律、法规,遵守社会道德、职业道德,贯彻执行国家方针政策,维护联盟成员的合法权益,秉承"守法、诚信、公正、科学"的职业准则,及时向政府有关部门反映成员的要求和意见。
三、联盟范畴
1、联盟内宣传国家对药用辅料行业发展的有关方针、政策;
2、逐步规范成员企业ICH研究及GMP符合性建设能力,促进行业健康有序发展;
3、建立意见反馈中心,协助成员向政府有关部门反映意见及要求,维护同盟的合法权益;
4、组织专业研讨会、行业交流会,法规宣讲会提高全行业人员的素质和业务水平;
5、开展咨询服务,向成员提供国内外注册法规信息和市场信息,为成员提供专业的国际注册指导及欧美高端法规市场的政策解读;
6、为联盟内成员提供共享平台,包括实验室研究,分析检测等;
7、帮助联盟内会员进行药用辅料的质量研究和选择;
8、印刷刊物,传递、反馈同行业和会员的信息,提高本协会和会员的知名度,推动各项任务的完成;
9、免费邀请会员参加联盟举办的各种形式的研讨会、论坛等活动;
10、 联盟组织机构。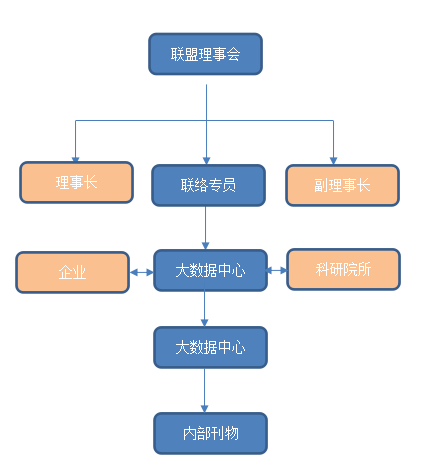
四、加入联盟
联盟会员分为团体会员、单位会员、个人会员。
申请加入联盟的条件:
1、拥护协会的章程;
2、有加入协会的意愿;
3、遵守职业道德,有良好的社会信誉;
4、依法登记的省、自治区、直辖市、副省级城市的医药相关协会,以及相关的行业协会,可以申请成为团体会员;
5、在中华人民共和国境内注册、从事药用辅料或者药品制剂生产获得生产许可证书的企业,可以申请成为单位会员;
6、已取得相关研究证书或具有教授、副教授、研究员、副研究员资格的内地居民,可以申请成为个人会员。
申请入会的程序:
1、填写、提交由联盟发布的《药用辅料质量研究共享联盟入会申请表》及有关证明材料;
2、经发起者讨论通过;
3、由发起者将入会企业或个人信息录入联盟数据库。
五、会员享有下列权利
1、保障和维护会员权利;
2、为会员提供国内外注册指导;
3、提供实验室检测支持;
4、获得行业动态信息;
5、列入协会网站会员通讯录;
6、参加会议、培训等活动享有优惠;
7、在网站期刊上刊登广告优先权和优惠;
8、优先处理疑难问题;
9、向联盟提出建议和意见;
10、入会自愿、退会自由。
六、会员履行下列义务
1、遵守联盟章程,执行联盟决议;
2、维护联盟的合法权益;
3、积极参与联盟组织的讨论会和交流会;
4、向协会反映情况,提供有关资料;
5、合理合法使用联盟内资源,不利用联盟资源进行非法牟利;
6、会员如有严重违反本章程的行为,经发起者组织会员表决通过,予以除名。
七、2018年度联盟福利
1、联盟成员可申请一次免费海外注册年度报告翻译;
2、联盟成员可申请一次免费注册资料的审核;
3、联盟成员可申请一次免费的研发设计方案;
4、联盟成员可申请二次半价海外注册项目;
5、联盟成员可申请二次半价辅料质量在评价项目;
6、联盟成员可申请一次免费FDA/EDQM质量体系符合性培训;
7、联盟成员可免费三次使用共享设备(物料、人员自备)。
八、药用辅料联盟共享平台设备列表
质量研究 | 仪器设备 |
用于混合物的分离、定性研究 | 液质联用(HPLC-MS) |
测包材内添加剂残留 | 气质联用(GC-MS) |
测金属元素 | 电感耦合等离子体(ICP) |
测有关物质、含量 | 液相色谱仪(HPLC) |
测残留溶剂、低沸点物质 | 气相色谱仪(GC) |
测紫外吸收 | 紫外分光光度计(UV) |
测红外吸收 | 红外分光光度计(IR) |
观察颗粒形貌,测粒度分布、粒径 | 颗粒成像仪 |
成膜性、稳定性、粒度 | 显微镜 |
测界面张力 | 表面/界面张力仪 |
测粉体流动性、筛分粒度、休止角、松密度、振实密度等 | 粉体综合测试仪 |
膨胀率 | 膨胀率测定仪 |
比表面积 | 比表面积测试仪 |
多晶型 | DSC或粉末衍射(可外检) |
测黏度 | 黏度计 |
测水分 | 水分测定仪 |
测熔点 | 熔点仪 |
测电导率 | 电导率仪 |
测渗透压 | 渗透压摩尔浓度测定仪 |
序号 | 试验名称 | 项目 | 备注 |
1 | 成立项目组 | 成立项目组,完成项目任务分配 | 双方成立项目组,项目组成员工作任务已分配,各个成员根据自己工作任务,搜索文献确定实验方案 |
2 | 文献查阅 | 质量研究文献、确定质量标准,研究内容,质量研究方案的完成、试剂购买。确定辅料的杂质谱,确定官方的杂质品及标准品,采购杂质,及原研辅料 | 质量标准的查找(当前国际先进通用的USP,BP,EP,JP,还有中国药典),杂质及原研或国际上的进口辅料 |
3 | 表征研究 | 结构确证。来自生物体的结构确证,采用ICH方法进行研究。 | 凯瑞德公司可以进行红外,质谱,晶型研究;其它联系符合国家局辅料申报要求资质的厂家的结构确证的单位或高校。 |
4 | 辅料原辅材料研究 | 根据生物来源产品ICH要求,制定物料的标准,验证分析方法 |
|
| 辅料 | 按先前找到的质量标准进行方法摸索及优化。其中有关物质项需确定所选用的有关物质条件能够将起始物料,中间体及工艺杂质和降解杂质都能检测出来,若检测不出来,我们会另建方法,对不能够检出的杂质进行单控;当工艺采用有机溶剂时需对残留溶剂进行控制;另外还需重点关注元素杂质、重金属、基因毒性杂质或微生物的质量研究 | 提供辅料合成的起始物料和中间体;微生物测定时需厂家完成。 |
6 | 功能性研究 | 根据厂家的要求,进行功能性研究 |
|
7 | 工艺优化 | 采用QBD的理念,结合厂家要求进行工艺优化 |
|
8 | 方法验证 | 方法摸索及确定 |
|
专属性、系统适用性 | |||
溶液稳定性 | |||
检测限、定量限和线性 | |||
加样回收率 | |||
重复性、中间精密度 | |||
耐用性 | |||
9 | 稳定性 | 影响因素试验,加速1,2,3,6月,长期3,6,9,12,18,24,36月试验 | 上报时候可以先提交六个月加速与六个月长期的稳定性 |
| 资料整理 | 据国家局的要求整理、撰写申报资料;准备现场核查用文件、资料 | 资料整理的时间可以在稳定性的过程中进行,等稳定性做完以后就可以申报 |
| 资料审核及申报 | 凯瑞德及厂家抽调技术及资料审评专家对资料进行一次审核,及二次审核定稿,并报国家局 |
|
本联盟最终解释权归石家庄凯瑞德医药科技发展有限公司所有。